
Photo: Wikimedia Commons/USFWS
Clonage, édition génétique et dévouement acharné offrent une lueur d’espoir à l’un des mammifères les plus menacés d’Amérique du Nord — et façonnent l’avenir de la science de la conservation.
Dans un centre discret niché dans les prairies de Virginie, deux petits furets ont ouvert les yeux à l’été 2024, sans se douter que leur venue au monde marquait une première mondiale. Avec leurs cernes noirs rappelant un masque de bandit, Sibert et Red Cloud sont des furets à pieds noirs (Mustela nigripes), l’un des mammifères les plus menacés du continent. Leur particularité ne réside pas uniquement dans leur rareté, mais aussi dans leur lignée : leur mère, Antonia, est un clone.
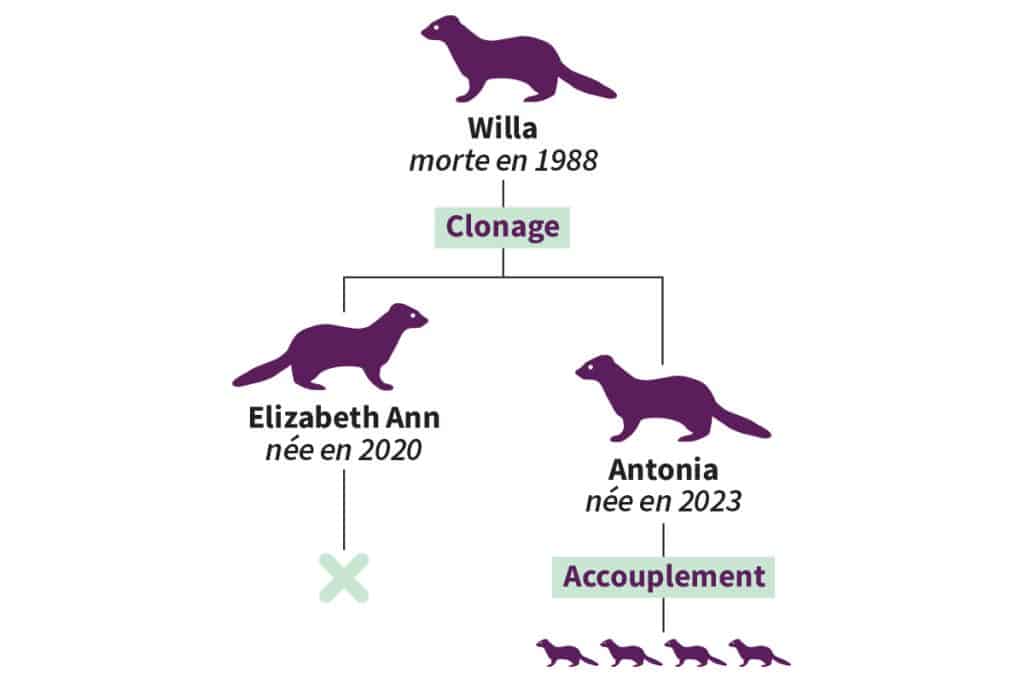
Née en 2023, Antonia a été conçue par clonage à partir de cellules prélevées sur une femelle nommée Willa, morte en captivité en 1988 sans descendance. Les cellules de Willa, préservées dans l’azote liquide grâce au programme « Frozen Zoo » du zoo de San Diego, sont devenues la source génétique du tout premier furet cloné dans un programme de conservation américain : Elizabeth Ann, née fin 2020. Lorsque celle-ci s’est révélée infertile, Antonia et sa sœur jumelle, Noreen, ont été conçues selon une méthode plus perfectionnée, sous l’égide de l’organisme Revive & Restore, qui a coordonné le projet et en a assuré la direction scientifique. Antonia a surpris les scientifiques en se reproduisant naturellement. Ses petits sont désormais les premiers descendants d’un animal cloné à naître dans un programme d’élevage conservatoire – c’est-à-dire qui consiste à élever des espèces menacées en captivité pour les relâcher ensuite.
Ben Novak, chercheur principal chez Revive & Restore, se réjouit de cette première mondiale. « Le plus encourageant dans cette histoire, c’est qu’Antonia a accepté son partenaire, s’est accouplée naturellement, a mis bas sans intervention humaine, puis a élevé elle-même ses petits jusqu’au sevrage. C’est exactement ce que nous espérons de ces technologies : que les animaux puissent s’intégrer pleinement et par eux-mêmes dans les systèmes écologiques naturels », dit-il.
Histoire d’une renaissance
 Autrefois répandu des Prairies canadiennes au nord du Mexique, le furet à pieds noirs a vu sa population s’effondrer au 20e siècle. L’une des causes principales fut la destruction des colonies de chiens de prairie, qui lui fournissent à la fois terrier et nourriture, par des campagnes d’empoisonnement visant à dégager les terres pour l’élevage. La perte d’habitat et l’arrivée de la peste sylvatique — une maladie introduite en 1900 par des puces venues d’Asie, transportées par des rats de navire — ont scellé le sort du furet. À la fin des années 1970, l’espèce était considérée comme éteinte.
Autrefois répandu des Prairies canadiennes au nord du Mexique, le furet à pieds noirs a vu sa population s’effondrer au 20e siècle. L’une des causes principales fut la destruction des colonies de chiens de prairie, qui lui fournissent à la fois terrier et nourriture, par des campagnes d’empoisonnement visant à dégager les terres pour l’élevage. La perte d’habitat et l’arrivée de la peste sylvatique — une maladie introduite en 1900 par des puces venues d’Asie, transportées par des rats de navire — ont scellé le sort du furet. À la fin des années 1970, l’espèce était considérée comme éteinte.
Mais en 1981, une petite population est redécouverte dans un ranch du Wyoming. Les derniers individus sont capturés pour lancer un ambitieux programme de reproduction. Seuls sept se reproduisent et donnent indirectement naissance, au fil des générations, à une descendance de 10 000 furets élevés en captivité. Plusieurs milliers d’entre eux ont été relâchés dans des dizaines de sites aux États-Unis, au Canada et au Mexique. Environ 300 à 400 individus survivent aujourd’hui en milieu sauvage, mais ils sont en sursis — d’autant qu’ils descendent tous des sept fondateurs d’origine. Un tel goulet d’étranglement génétique augmente les risques d’infertilité, de maladies et de faible capacité d’adaptation. Aucune malformation n’a été observée à ce jour, mais les scientifiques constatent déjà une baisse de la fertilité chez les femelles. L’arrivée d’Antonia change la donne. En tant que descendante de Willa, elle réintroduit dans le programme d’élevage des variations génétiques absentes des populations actuelles — une diversité environ trois fois plus élevée que celle observée chez les furets vivant aujourd’hui à l’état sauvage.
« Avant d’introduire ces animaux clonés, et leurs gènes, dans les populations sauvages, nous évaluerons le développement et le comportement de leur descendance, indique Oliver Ryder, directeur de la conservation génétique à la San Diego Zoo Wildlife Alliance. Noreen et Antonia sont encore en croissance, mais Antonia a déjà eu des petits. C’est bon signe. »
La piste de l’autovaccination
En collaboration avec des scientifiques du MIT, l’organisme Revive & Restore travaille sur une technique innovante de vaccin génétique contre la peste sylvatique. Le principe : modifier le génome de l’animal pour y insérer un code génétique complexe, qui produit temporairement un antigène vaccinal dans les muscles de l’animal à un moment précis de sa vie. Ce code génétique ajouté inclut également un mécanisme d’auto-suppression, conçu pour éliminer la séquence vaccinale des cellules où elle s’est activée. Ainsi, la séquence vaccinale s’éliminerait du génome des cellules de muscles, mais demeurerait présente ailleurs dans l’organisme – en particulier dans les cellules reproductrices. Elle resterait donc transmissible à la descendance, qui serait à son tour capable de produire son propre vaccin.
Un chapitre canadien
Les efforts de réintroduction ont dépassé les frontières, mobilisant scientifiques et spécialistes de la conservation des deux côtés de la frontière. Le défi ne consiste pas seulement à relâcher les animaux dans des milieux propices, mais aussi à garantir leur survie dans un contexte écologique et politique incertain. Le Canada, lui aussi, a tenté de réintroduire l’espèce. En 2009, des individus ont été relâchés dans le parc national des Prairies, en Saskatchewan. Mais la population a rapidement disparu, probablement en raison d’épidémies de peste et de l’effondrement des colonies de chiens de prairie. Les zoos de Toronto et de Calgary participent encore à l’élevage en captivité pour soutenir les efforts américains.
Programmer l’immunité
Pour le rétablissement de l’espèce, le contrôle des maladies est aussi devenu une priorité. Les équipes de conservation mènent une lutte constante contre la peste sylvatique, qui se propage rapidement dans les colonies de chiens de prairie, les décimant parfois en quelques semaines. Avec, en cascade, la disparition des furets qui en dépendent – et qui peuvent eux aussi contracter la maladie.
Le biologiste Travis Livieri, de l’organisme Prairie Wildlife Research, a consacré près de 30 ans de sa vie à protéger les furets à pieds noirs. Les furets nés en captivité sont vaccinés ; ceux nés dans la nature doivent être capturés pour l’être — une tâche exigeante pour les équipes de terrain. Son équipe, basée dans le Conata Basin, au Dakota du Sud, les capture la nuit, les vaccine, puis les relâche. Une opération lourde, chaque animal devant recevoir deux doses.
Ici aussi, la génétique pourrait donner un coup de pouce. L’équipe de Ben Novak développe ce qu’elle appelle des « furets auto-vaccinants », grâce à une technique encore très expérimentale (voir encadré).
Autre piste : faire intervenir les furets domestiques, qui sont naturellement immunisés. Les scientifiques pensent avoir identifié la mutation responsable de leur protection. Si cela se confirme, elle pourrait un jour être intégrée dans les génomes des furets sauvages grâce à l’édition génétique avancée.
Des efforts vains ?
Mais à quel point la technologie peut-elle compenser la destruction des écosystèmes ? Les percées scientifiques sont prometteuses, mais pas miraculeuses. Selon Kristy Bly, du Fonds mondial pour la nature (WWF), il faut commencer par restaurer des écosystèmes de chiens de praire si on veut sauver le furet. Elle estime que 4000 hectares bien gérés – environ un dixième de l’île de Montréal –, répartis sur au moins 30 sites, suffiraient à soutenir une population de furets génétiquement diversifiée et résistante aux maladies.

Même si les individus clonés ou génétiquement modifiés prospèrent en captivité, leur retour à la nature sera progressif – et les plus précieux sur le plan génétique resteront dans les centres d’élevage.
« En réalité, nous allons travailler avec les furets à pieds noirs pendant encore 15 à 20 ans pour déployer ces solutions, accroître leur diversité génétique et surmonter la maladie, conclut Ben Novak. Ce que nous apprenons ici pourrait servir à beaucoup d’autres espèces. »

Photo: Alamay
Faire revivre une espèce éteinte ?
Avez-vous déjà entendu parler de projets de « désextinction », qui veulent faire revenir à la vie des espèces disparues ?
Là aussi, la génétique a un rôle central. Mais plutôt que d’utiliser des cellules congelées, rarement disponibles pour des espèces éteintes, on se base plutôt sur des fragments d’ADN trouvés sur des fossiles. C’est ce que fait Colossal Biosciences, qui a annoncé en avril dernier avoir ressuscité le loup sinistre, ou dire wolf, disparu il y a plus de 10 000 ans.
L’entreprise américaine a affirmé avoir séquencé le génome complet du loup sinistre à l’aide de matériel génétique extrait d’une dent et d’un crâne fossilisé. Puisque l’ADN ancien est trop endommagé pour permettre le clonage traditionnel, les biologistes de Colossal Biosciences ont plutôt comparé ce génome avec celui du loup gris, qui partage selon eux 99,5 % de son code génétique avec le loup sinistre. Ils ont ensuite introduit une vingtaine de modifications dans le génome d’un loup gris pour lui transmettre certaines caractéristiques physiques du loup disparu, comme la taille ou la forme des oreilles.
Trois louveteaux portant ce code génétique sont nés en octobre dernier. Mais de nombreux scientifiques ont souligné que ces loups gris génétiquement modifiés sont très loin des véritables loups sinistres. Selon une analyse génétique de 2021 (révisée par les pairs, contrairement aux travaux de Colossal Biosciences), le loup sinistre aurait été en réalité plus proche du chacal et du chien sauvage africain que des loups. L’étude indique aussi qu’il aurait pu avoir un pelage roux et l’apparence d’un coyote géant. Peu à voir, finalement, avec le loup blanc majestueux vu dans Le trône de fer…
— Louise Toutée







