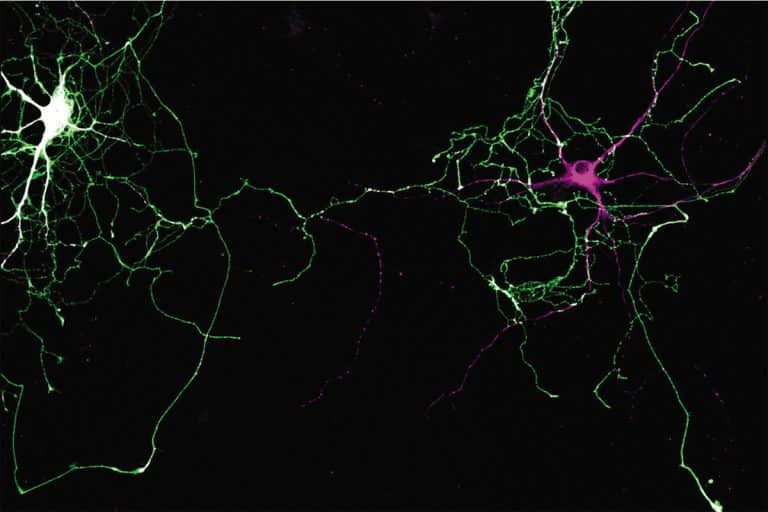
Cocristaux à base d’antimoine. Image: Filip Topic
En plus de transformer notre perception de la façon dont les molécules se combinent et s’organisent, cette découverte ouvrirait la porte à la conception de matériaux semi-conducteurs et électroniques plus résistants à l’humidité.
Une molécule est un assemblage d’atomes fortement soudés les uns aux autres. Deux atomes d’hydrogène fixés fermement à un atome d’oxygène forment une molécule d’eau : H 2 O. Mais il existe aussi des forces d’attraction entre les molécules. Dans le cas de l’eau, l’atome d’hydrogène d’une molécule est attiré par l’atome d’oxygène d’une autre. Loin d’avoir la force d’une soudure, ces liaisons hydrogène entre molécules sont plutôt comme des aimants de frigo et se comptent par trilliards dans une goutte.
Rassembleuses, les liaisons hydrogène peuvent réunir des molécules contenant des éléments légers : azote, fluor, oxygène… Mais les choses se compliquent avec les éléments lourds. Or, une autre forme de liaison intermoléculaire demeure peu explorée : les liaison halogène. Elles sont possibles avec les molécules renfermant du chlore, du brome ou de l’iode. Jusqu’à récemment, on ne les avait observées qu’en face d’atomes légers.
Souhaitant rapprocher des éléments plus lourds, Tomislav Friščić, professeur au Département de chimie de l’Université McGill, a plongé dans la 15 e colonne du tableau périodique. Le phosphore, l’arsenic ou l’antimoine accepteraient-ils de serrer une main tendue par un atome d’iode ?